الکتروشیمی در فرآوری مواد معدنی:
بررسی کاربردها، روشها و نقش کلیدی در صنایع معدنی
مقدمه:
الکتروشیمی شاخهای از علم شیمی است که به بررسی واکنشهای شیمیایی همراه با انتقال الکترون حین واکنش میپردازد. این علم، نقش پررنگی در صنایع مختلف از جمله متالورژی، انرژی، تصفیه آب و بهویژه فرآوری مواد معدنی ایفا میکند. در فرآوری مواد معدنی، الکتروشیمی بهعنوان ابزاری مؤثر برای جداسازی، بازیابی و تصفیه فلزات از سنگهای معدنی به کار میرود. و به طور کلی یکی از مراحل پایانی دستیابی به فلز مورد نظر است.

کاربرد الکتروشیمی در فرایند فولادسازی
مبانی:
عدد اکسایش (Oxidation Number) چیست؟
عدد اکسایش عددی است که نشان میدهد یک اتم در یک ترکیب شیمیایی چه تعداد الکترون از دست داده یا به دست آورده است (یا فرض میشود که از دست داده یا گرفته) تا به آن وضعیت رسیده باشد. این عدد معیاری برای تعیین درجه اکسایش یا کاهش یک عنصر در یک واکنش الکتروشیمایی است.
عدد اکسایش میتواند:
مثبت باشد → یعنی اتم الکترون از دست داده است (اکسید شده)
منفی باشد → یعنی اتم الکترون به دست آورده است (احیا شده)
صفر باشد → در اتمهای خنثی یا عناصر آزاد (مثل O₂، H₂)
واکنشهای الکتروشیمیایی (Redox Reactions) به دو دستهی اصلی اکسیداسیون (افزایش) و احیا (کاهش) تقسیم میشوند. در فرآیند اکسیداسیون، یک ماده الکترون از دست میدهد و در نتیجه عدد اکسایش آن افزایش مییابد. در مقابل، در واکنش احیا، مادهای الکترون دریافت میکند و عدد اکسایش آن کاهش مییابد. این دو واکنش همواره به صورت همزمان در یک سیستم بسته (سلول الکتروشیمیایی) رخ میدهند.
سلول الکتروشیمیایی شامل دو نیمسلول آندی و کاتدی است.
هر نیمسلول نیز شامل یک الکترود (جامد رسانا) و یک محلول الکترولیت حاوی یونهای مربوط به آن الکترود میباشد.
در نیمسلول آندی، الکترود آند قرار دارد که در آن واکنش اکسیداسیون رخ میدهد؛ یعنی ماده الکترون از دست میدهد. این نیمسلول معمولاً شامل یک فلز (مثلاً Cu یا Zn) و محلولی از نمک آن فلز (مثلاً CuSO₄ یا ZnSO₄) است.
در نیمسلول کاتدی، الکترود کاتد قرار دارد که در آن واکنش احیا انجام میشود؛ یعنی یونهای فلزی موجود در محلول، الکترون دریافت کرده و به فلز خالص تبدیل میشوند.
در سیستمهای الکتروشیمیایی، دو الکترود به نامهای آند و کاتد نقش اصلی را ایفا میکنند:
آند (Anode): محل وقوع واکنش اکسیداسیون است؛ در اینجا عنصر الکترون از دست میدهد.
کاتد (Cathode): محل وقوع واکنش احیاست؛ در این نقطه یونهای فلزی موجود در محلول، الکترون دریافت کرده و به فلز خالص تبدیل میشوند.
جهت حرکت الکترون ها (قراردادی و واقعی):
جهت قرادادری جریان الکتریکی
جهتی است که از قطب مثبت منبع (مثلاً باتری) به سمت قطب منفی در نظر گرفته میشود.
تاریخچه: این جهتگیری در قرن هجدهم و قبل از کشف الکترونها توسط بنجامین فرانکلین پیشنهاد شد. در آن زمان تصور میشد “سیالی از بار مثبت” حرکت میکند.
- کاربرد: هنوز هم در رسم مدارها، تحلیل مدارات الکتریکی، و محاسبات مهندسی از این جهت استفاده میشود. به نوعی یک قرارداد جهانی است.
جهت واقعی حرکت الکترونها
تعریف: جهت واقعی حرکت الکترونها، جهتی است که الکترونهای آزاد از قطب منفی (مثلاً سر منفی باتری) به سمت قطب مثبت حرکت میکنند.
علت: الکترونها دارای بار منفی هستند و توسط میدان الکتریکی از سمت منفی به سمت مثبت رانده میشوند.
ویژگی: این جهت برخلاف جهت قراردادی جریان است.
در واقع جهت جریان قراردادی که در گذشته اتفاق افتاده، جهت حرکت بارهای مثبت است (چون هنوز الکترون ها شناخته نشده بودند)،
و بعدا که فهمیدند الکترون وجود دارد جهت حرکت الکترون ها میشه مخالف این جهت جریان. ولی در واقع دو مفهوم نه تنها متضاد نیستن. بلکه تکمیل کننده هم هستند.
به خاطر همین، قطب مثبت باتری در قدیم یعنی تجمع بارهای مثبت یا کمبود بار منفی و قطب منفی یعنی تجمع بار منفی و کمبود بار مثبت.
در نتیجه خروج الکترون ها چه در قرارداد و چه در واقعیت میشود همیشه قطب منفی است و ورود الکترون ها قطب مثبت است.
خلاصه: در قرارداد جهت جریان الکتریکی را جهت حرکت بارهای مثبت در نظر گرفتند ولی بعدها فهمیدند که جریان الکتریکی را بارهای منفی ایجاد می کنند و بار مثبت حرکت نمی کند.
اینجاست که مفهوم پتانسیل الکتریکی نیز بیان می شود: الکترون ها از پتانسیل بیشتر (قطب منفی) به پتانسیل کمتر (قطب مثبت) حرکت می کنند. قطب منفی یعنی پتانسیل بالاتر، تمایل به دفع الکترون دارد.
پتانسیل الکتریکی و سری الکتروشیمایی عناصر:
پتانسیل الکتریکی (یا اختلاف پتانسیل الکتروشیمیایی) نیروی محرکهای است که باعث حرکت الکترونها از یک الکترود به الکترود دیگر در یک سلول الکتروشیمیایی میشود. این پتانسیل، تابعی از واکنشهای اکسیداسیون و احیا در نیمسلولها است و تعیینکننده میزان انرژی آزاد که سلول میتواند تولید کند، میباشد.
پتانسیل استاندارد الکترود (E°)
هر نیمسلول دارای یک پتانسیل استاندارد الکترود است که نسبت به یک الکترود مرجع (معمولاً الکترود استاندارد هیدروژن) اندازهگیری میشود. (هیدروژن صفر است)
این مقدار در شرایط استاندارد (دمای ۲۵ درجه سانتیگراد، فشار ۱ اتمسفر، و غلظت یونها ۱ مول بر لیتر) تعیین میگردد.
پتانسیل استاندارد هر نیمسلول نشاندهنده تمایل آن برای اکسید شدن یا احیا شدن است.
به همین علت در سری الکتروشیمیایی، پتانسیلهای اکسایش و کاهش به صورت جداگانه ذکر میشوند. این دو مقدار از نظر عددی برابر هستند اما دارای علامتهای مخالف میباشند؛ به این معنی که:
پتانسیل کاهش نشاندهنده تمایل یک گونه برای دریافت الکترون و احیا شدن است.
پتانسیل اکسایش نشاندهنده تمایل همان گونه برای از دست دادن الکترون و اکسید شدن میباشد.
برای هر واکنش الکتروشیمایی، واکنش اکسیداسیون عکس واکنش کاهش است و به همین دلیل پتانسیل اکسایش، منفی پتانسیل کاهش آن واکنش خواهد بود.
یک باتری در واقع یک سلول الکتروشیمایی است که مولد اختلاف پتانسیل (جریان الکتریکی) در یک مدار است. یعنی از قطب منفی که پتانسیل اکسایش آن بیشتر است الکترون به سمت قطب مثبت با پتانسیل کمتر میرود، به تعبیری دیگر الکترون از قطب منفی با پتانسیل کاهش کمتر (تمایل به جذب الکترون کمتر) به قطب مثبت با پتانسیل کاهش بیشتر می رود. و دلیل این اختلاف پتانسیل ایجاد شده در مدار باتری است. مثل یک جرثقبل که یک منبع آب را بالا برده و اختلاف پتانسیل گرانشی ایجاد کرده.
اکسید کننده و احیا کننده:
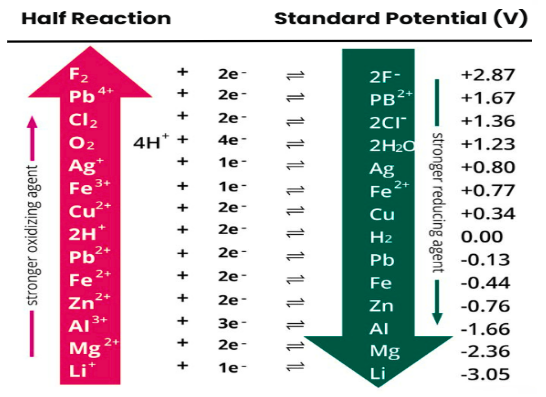
در سری الکتروشیمایی که معمولا به صورت پتانسیل کاهشی از بالا به پایین نزولی است، عناصر بالای هیدروژن اکسیدکننده بوده (عامل اکسنده) و پایین هیدروژن احیا کننده می باشند.
مفهوم الکترونگاتیوی و پتانسیل کاهشی دو مفهوم همراستا هستند، هر چه یک عنصر الکترونگاتیو تر (به سمت راست و بالای جدول تناوبی) تمایل به احیا آن بیشتر و در نتیجه عامل اکسید کننده است.
در فرآوری مواد معدنی، این اصل پایه برای استخراج و تصفیه فلزات از محلولهای شیمیایی (مثلاً پس از لیچینگ) به کار میرود. بسته به نوع فلز و شرایط فرایند، انتخاب مواد الکترود، چگالی جریان، pH و نوع الکترولیت میتواند نقش تعیینکنندهای در بازده واکنش داشته باشد.
در صنایع معدنی، روشهای الکتروشیمیایی بسته به فاز واکنشدهندهها به دو حوزه اصلی تقسیم میشوند:
۱- الکتروشیمی در فاز محلول
۲- الکتروشیمی در فاز جامد
🔹 ۱. الکتروشیمی در فاز محلول (هیدرومتالورژی)
در این حالت، یونهای فلزی در فاز آبی یا محلول الکترولیت قرار دارند و با اعمال جریان الکتریکی این یونها در سطح الکترود احیا یا اکسید میشوند. همچنین در برخی فرایند های انحلال (لیچینگ) نیز واکنش های الکتروشمیایی حاکم است.
✅ الف) لیچینگ (Leaching)
در برخی فرآیندهای هیدرومتالورژیکی، انحلال کانسنگهای مقاوم به روشهای معمول تنها در حضور عوامل اکسنده یا احیاکننده مؤثر انجام میگیرد. این مواد با تغییر عدد اکسایش عناصر موجود در کانی، مسیر واکنش را تسهیل میکنند و انحلال یونهای فلزی را امکانپذیر میسازند.
بهعنوان مثال، در فرآیند انحلال کنسانتره کالکوپیریت (CuFeS₂) که یکی از مقاومترین و پایدارترین کانیهای مس محسوب میشود، از عوامل اکسنده قوی مانند یون فریک (Fe³⁺) و آب اکسیژنه (H₂O₂) استفاده میشود. این ترکیبات با اکسید کردن یونهای گوگرد و آهن موجود در ساختار کالکوپیریت، پیوندهای درونی کانی را شکسته و باعث آزاد شدن یونهای مس (Cu²⁺) در محلول میشوند.
✅ الف) الکترووینینگ (Electrowinning)
هدف: استخراج فلزات از محلولهای آبی حاصل از لیچینگ
مکانیزم: یونهای فلزی (مثل Cu²⁺، Zn²⁺، Ni²⁺) در محلول، در کاتد با دریافت الکترون به فلز خالص تبدیل میشوند.
- محلول حاوی یون های مورد نظر (الکترولیت) درون سلول قرار گرفته و توسط اعمال جریان الکتریکی بر روی کاتد رسوب می کنند.
کاربردها: استخراج مس، روی، نیکل، کبالت، طلا
ویژگی: فلز مستقیماً از محلول به شکل فلز جامد روی کاتد رسوب میکند.
✅ ب) الکتروریفاینینگ (Electrorefining)
هدف: تصفیه فلزات ناخالص و تولید فلز با خلوص بالا
مکانیزم: فلز ناخالص در اینجا حذف شده و تنها فلز خالص در کاتد رسوب میگردد.
- کاربردها: تصفیه مس، نیکل، سرب، نقره
🔹 ۲. الکتروشیمی در فاز جامد (پیرومتالورژی)
در این حالت، واکنشهای الکتروشیمیایی در فاز جامد انجام میشوند یا تحت تأثیر شرایط خاص، فاز جامد در محیطی اکسیدی یا احیایی دچار واکنش میشود. این حوزه کمتر به صورت مستقیم الکترولیتی است، اما پایههای الکتروشیمیایی دارد.
✅ الف) تشویه اکسیدی (Oxidation Roasting)
فرایند: اکسید کردن سولفیدهای فلزی (مثل FeS₂، ZnS، CuFeS₂) با هدف تبدیل آنها به اکسیدها یا سولفاتهای محلولپذیر.
واکنشها در حضور هوا یا اکسیژن انجام میشود اما در شرایط کنترلشده از نظر پتانسیل الکترونی، گاهی با کمک الکترودهای جامد برای پایش واکنشها.
✅ ب) تشویه احیایی (Reduction Roasting)
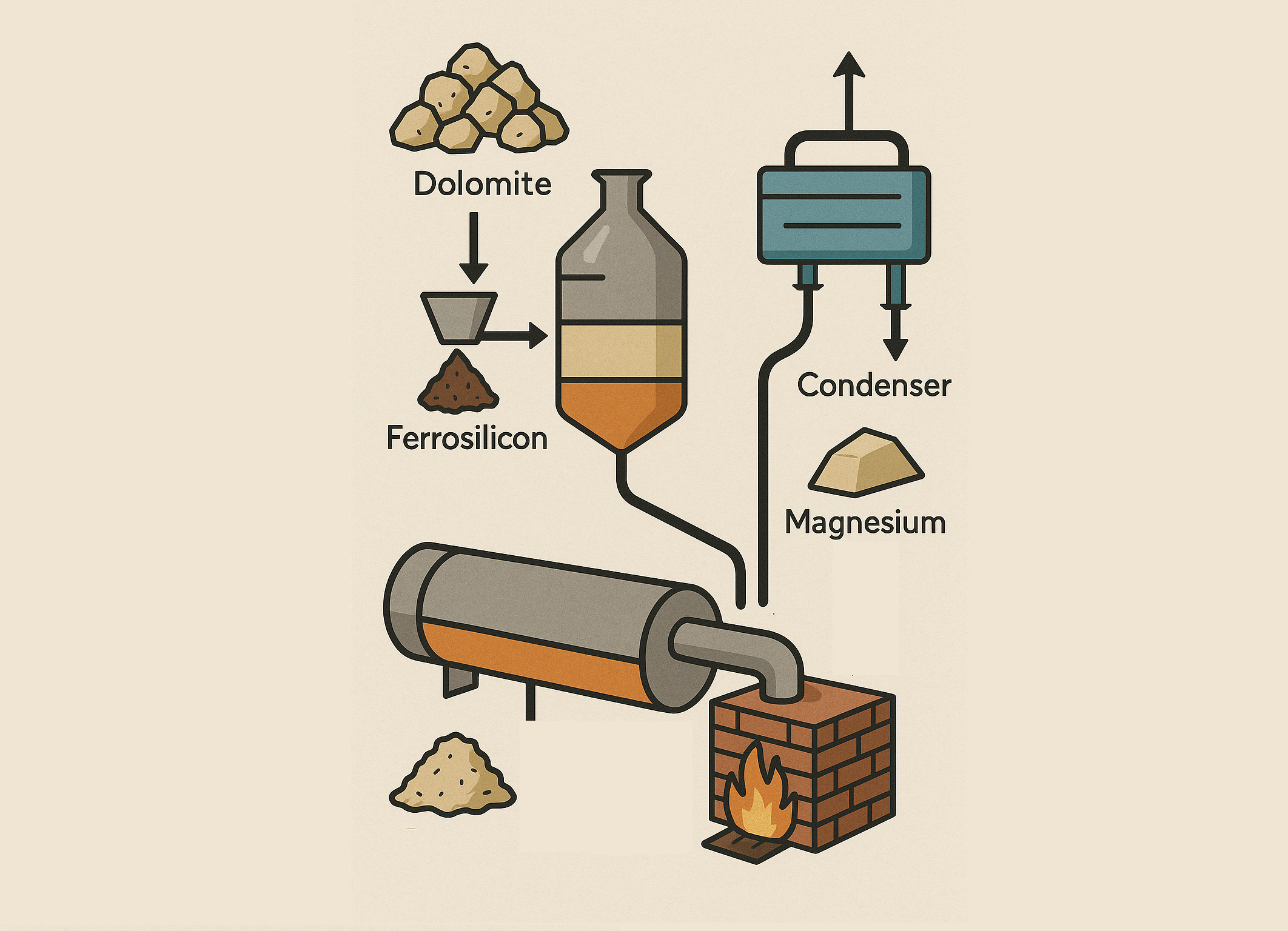
در این روش، اکسیدهای فلزی در حضور مواد کاهنده (مثل کربن یا گاز H₂) کاهش یافته و به فلز تبدیل میشوند. مانند تولید روی به روش ولز یا تولید منیزیم به روش پیجن.
نمودار پوربه (Pourbaix diagram):
نمودار پوربکس (پتانسیل–pH) ابزاری مهم در مهندسی متالورژی و فرآوری مواد معدنی است که با نمایش پایداری فازهای مختلف یک فلز، به انتخاب شرایط مناسب برای لیچینگ، استخراج، تصفیه و جداسازی فلزات کمک میکند. این نمودار امکان پیشبینی رفتار ترمودینامیکی یونها، جلوگیری از خوردگی تجهیزات، انتخاب عوامل اکسنده یا احیاکننده مناسب، و کنترل رسوبگذاری یا حل شدن فلزات را فراهم میسازد. بهطور کلی، استفاده از نمودار Pourbaix موجب بهینهسازی و افزایش بازده در فرآیندهای هیدرومتالورژیکی و الکتروشیمیایی میشود. در نمودار پوربه محور افقی pH و محور قائم Eh است. این نمودار شرایط ترمودینامیکی پایداری هر فاز را نشان می دهد.
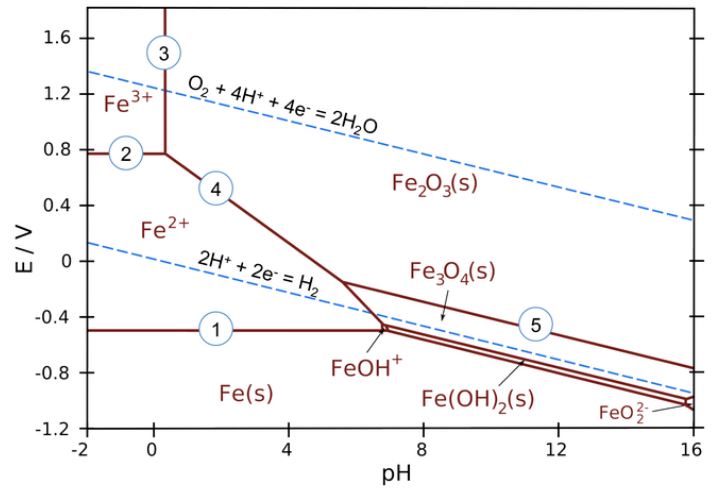
نمودار پوربه آهن برای غلظت یونی یک دهم میلی مولار
رابطه فارادی:
رابطه فارادی نشان میدهد که مقدار مادهای که در یک واکنش الکترولیتی تولید یا مصرف میشود، مستقیماً با مقدار بار الکتریکی عبوری متناسب است. فرض کنید میخواهیم با استفاده از جریان برق، مس را از محلول حاوی یونهای آن استخراج کنیم. یونهای مس در این محلول به صورت مس (II) وجود دارند، یعنی برای تبدیل هر یون مس به فلز جامد، باید دو الکترون به آن داده شود.

چرا غلظت در نمودار پوربه اهمیت دارد؟
نمودار پوربکس بر پایه معادله نرنست ترسیم میشود که در آن پتانسیل الکتروشیمیایی وابسته به غلظت یونها است. تغییر غلظت یونی، موقعیت مرزهای بین فازهای مختلف (مانند Fe، Fe²⁺، Fe³⁺، Fe(OH)₃ و غیره) را روی نمودار جابهجا میکند.
معادله نرنست چیست؟
معادله نرنست رابطهای است که پتانسیل الکتروشیمیایی یک واکنش را با غلظت گونههای شرکتکننده در واکنش مرتبط میکند. این معادله نشان میدهد که هرچه غلظت یونهای واکنشدهنده بیشتر باشد، پتانسیل الکترودی تغییر میکند. به زبان ساده، نرنست کمک میکند تا بفهمیم در شرایط غیر استاندارد (مثلاً غلظتهای کم یا زیاد)، ولتاژ یا تمایل یک واکنش اکسایش یا کاهش چقدر تغییر میکند.نمودار پوربکس بر پایه معادله نرنست ترسیم میشود که در آن پتانسیل الکتروشیمیایی وابسته به غلظت یونها است. تغییر غلظت یونی، موقعیت مرزهای بین فازهای مختلف (مانند Fe، Fe²⁺، Fe³⁺، Fe(OH)₃ و غیره) را روی نمودار جابهجا میکند.
سمنتاسیون یعنی چه؟
سمنتاسیون (Cementation) فرایندی شیمیایی در متالورژی است که طی آن یک فلز با احیای یونهای فلز دیگر توسط فلزی با پتانسیل احیای بالاتر، از محلول بازیابی میشود (سری الکتروشیمایی). در این واکنش، فلز قویتر اکسید شده و فلز ضعیفتر بهصورت جامد رسوب میکند.
مثلاً در بازیابی مس از محلول، با وارد کردن فلز آهن، یونهای Cu²⁺ احیا شده و به صورت فلز مس رسوب میکنند، در حالی که آهن به Fe²⁺ تبدیل میشود. این روش ساده، کمهزینه و در بسیاری از فرآیندهای صنعتی، بهویژه در استخراج فلزات از محلولهای لیچینگ، کاربرد دارد.









دیدگاه ها
笑赚网
我来看看是咋么回事
Make Money At Home
Hi, how have you been lately?